


بدأت كاتالين كاريكو، عالمة الكيمياء الحيوية المجرية، العمل على تقنية mRNA في وقت مبكر من 1989؛ قبل أن تنتج بحثها الأهم في جامعة بنسلفانيا في منتصف العقد الأول من القرن الحالي.
كانت الفكرة وراء تطويع mRNA كدواء بسيطة بشكل مذهل: إنه الجزيء الذي تستخدمه الخلايا الخاصة بك لنقل التعليمات من جيناتك، مكتوبة بلغة كيميائية بسيطة من أربعة أحرف.
إذا كان بإمكانك تصنيعه في المختبر وتسليمه إلى الخلايا، يمكنك نظريًا أن تطلب منهم صنع أداة معينة - مستضد فيروسي، أو جزيء مانع للسرطان، أو المزيد من أنسجة القلب - كل ذلك بلغتهم الخاصة.
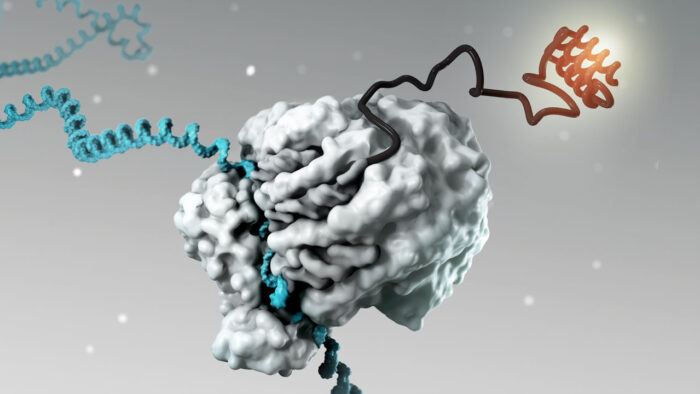
لكن، مثل العديد من الافتراضات الجذابة نظريًا، واجه التطبيق مشكلات ضخمة عمليًا:
يرفض الجسم بعنف قبول mRNA من مصادر خارجية - ربما لتجنب التقاط الفيروسات ومسببات الأمراض الأخرى - وغالبًا ما أثبت mRNA أنه سام للغاية لدرجة أنه قتل حيوانات المختبر التي خضع للاختبار عليها.
لسنوات، كانت هذه عقبة كبيرة جعلت فقط القليل من العلماء فكروا في استخدامها للقاحات. ديفيد سكيلز، أستاذ الطب المساعد في جامعة كورنيل الذي عمل مع كاريكو كطالب يقول:
"كان الأمر نظريًا جدًا في ذلك الوقت، ولم يكن أحد يفعل هذه الأشياء حقًا".
كاريكو نفسها علقت: "لم يكن يمكننا أن نحلم باستخدامه على البشر".
من خلال العمل مع عالم المناعة درو وايزمان في جامعة بنسلفانيا في أوائل العقد الأول من القرن الحادي والعشرين، صممت كاريكو جزيئات mRNA اصطناعية يمكن أن تتجنب دفاعات الجسم.
يقول وايزمان إنها كانت عملية شاقة قتلت الكثير من الفئران قبل أن يكتشفوا أخيرًا الصيغة الناجحة في 2004، لتتفتح بهذا خطوط الاتصال بين خلايانا ورسائل mRNA التي أنشأها العلماء.
تعتقد كاريكو دائمًا أن mRNA يمكنه فعل أي شيء: "كنت أذهب إلى اجتماعات علمية وأتواصل مع الباحثين لأقول: ما الذي تعمل عليه؟ ربما يمكن لتقنية RNA هذه أن تساعد - مهما كان المرض، حتى الصلع. تقول ضاحكة: "ربما اعتقدوا جميعًا أنني مجنونة".

نجحت التجربة، لكنها واجهت مشكلة التمويل. كانت مؤسسات الأبحاث الطبية مهتمة باختبار التقنية الوليدة ضد الأمراض الفتاكة التي تجاهلتها صناعة الأدوية إلى حد كبير، مثل حمى الضنك أو حمى لاسا. لكن المشكلة دائمًا أن شركات الأدوية الكبرى لم تكن متحمسة لتمويل تلك الأبحاث "الخيالية".
لكن شركات أصغر قررت الرهان، بينها بيونتك ومودرنا. كلتاهما لم تكونا اسمًا مألوفًا. لم ينتج أي منهما دواء واحدا توافق عليه السلطات الصحية من قبل.
لكنهما راهنتا منذ فترة طويلة على تقنية mRNA، ليتبين لاحقًا أنهما أجادا الرهان، وأن mRNA شيء نادر تمامًا في عالم العلوم والطب: تقنية واعدة وتحويلية لم تنجح فقط من أول اختبار كبير لها، لكنها حققت أكثر من توقعات معظم الناس.
رغم ذلك استمر ضعف التمويل، وعجز التقنية نفسها عن إثبات أي نجاح يذكر، كاد رعاتها أنفسهم أن يصابوا بالإحباط. هنا بدأت جائحة كورونا، وبحث العالم عن أي أمل ممكن لإنتاج اللقاح سريعًا، فضخت الاستثمارات في أية تقنية متاحة، وحصلت mRNA على نصيبها.
رعاتها أنفسهم لم يكونوا واثقين تماما في إمكانية النجاح!
حتى أوغور شاهين، المؤسس المشارك والرئيس التنفيذي لشركة بيونتيك، الذي رعى لقاح فايزر منذ مراحله الأولى، كانت لديه بعض الشكوك.
يقول إن موظفيه كانوا يخبرونه دائمًا أن اللقاح "شبه مثالي" من الناحية المناعية، لكنه كان دائم الشك في أنها ستعمل ضد "الوحش الكامن هناك".
لكن قواعد اللعبة تغيرت لأول مرة في 9 نوفمبر 2020، بعد ثلاثة أشهر من التجربة السريرية النهائية، حيث تلقى الأخبار السارة أخيرًا "الفعالية تجاوزت 90%". والخبر الأكثر سعادة للمجتمع العلمي أن لقاح مودرنا الذي يستخدم نفس التقنية حقق نجاحًا مماثلًا.

الآن، رأت الصناعة فرصة ضخمة، ما يحمل معه فرصًا كبيرة لتسريع البحث عن الأحلام العلمية التي طال أمدها: لقاح محسن ضد الإنفلونزا، أو لقاح فعال ضد فيروس نقص المناعة البشرية.
أميش أدالجا، خبير الأمراض الناشئة في مركز جونز هوبكنز، يقول إن تقنية mRNA تبشر بتحول كل التطبيقات التي كان الباحثون يحلمون بتمويلها إلى جزء من الحياة اليومية".
يضيف: "عندما يكتبون تاريخ اللقاحات، فمن المحتمل أن تكون هذه نقطة تحول".
يشبه هذا المجال أحيانًا المرحلة المبكرة من اندفاع الذهب، حيث تستقطب شركات الأدوية العملاقة الباحثين الواعدين مقابل عقود ضخمة. سانوفي دفعت مؤخرًا 425 مليون دولار للمشاركة مع شركة أمريكية صغيرة لتكنولوجيا mRNA تسمى ترانسليت بايو، بينما دفعت جي إس كيه 294 مليون دولار للعمل مع شركة CureVac الألمانية.
هارتاج سينغ، محلل الصناعة في شركة أوبنهايمر وشركاه، يقول إن كل تلك الأرقام لا تعني إلا أن التغيير قادم. لقاحات mRNA كانت الفائز الأكبر في معركة كورونا، وخلال سنوات قليلة سترث منصات اللقاحات القديمة كليًا، أو على الأقل ستقلصها إلى حد كبير.

عكس الأيام الأولى لأبحاث mRNA، لن ننتظر عقودًا للاختبار الكبير التالي. ربما يكون الاختراق الكبير القادم للقاح mRNA ضد مرض مألوف جدًا: الأنفلونزا هي الهدف الأول.. مرض يعتبره معظم الناس تحت السيطرة ، لكنه يقتل أكثر من 300,000 شخص في جميع أنحاء العالم في معظم السنوات، رغم ضخ أكثر من مليار جرعة لقاح سنويًا.
تقول مراكز السيطرة على الأمراض والوقاية منها (CDC) إنها نادرًا ما تحقق حماية بنسبة 50%، انخفضت إلى 29% في موسم 2018-2019، بينما تصل بالكاد إلى 10% في بعض السنوات.
أحد العلماء الذي يطارد هذا الحلم هو نوربرت باردي حتى قبل جائحة كورونا، إذ كان مقتنعًا أن mRNA قادرة على حل مشكلة ضعف اللقاح الحالي.
مشكلة لقاحات الأنفلونزا الحالية في عدم التطابق بين الطبيعة المراوغة لفيروس الأنفلونزا والطريقة القديمة والبطيئة التي نستخدمها لصنع لقاح ضده، ليواصل الفيروس التحول خلال مرحلة تصنيع اللقاح الجديد،
كان الأمر أشبه بـ "مطاردة هدف متحرك"، بوصف الرئيس السابق لقسم اللقاحات في السي دي سي، بروس جيلين. يبدو أن mRNA مصممة لتغيير المسار؛ إذ يحول جسمك إلى مصنع للقاحات، أكثر كفاءة بمليون مرة من أي مختبر على الأرض، بوصف آنا بلاكني، باحثة الحمض النووي الريبي في جامعة كولومبيا البريطانية.
وتتوقع بيونتك أن تبدأ التجارب البشرية على اللقاح الجديد في وقت لاحق من 2021.
لكن لقاحات mRNA لن تتوقف عند الأنفلونزا. ليندا ستيوارت، نائبة مدير اللقاحات في مؤسسة جيتس، تقول إن الهدف اللاحق سيكون "المشكلات والأمراض الحقيقية، الصعبة، والمستعصية".
ولأن العلم لم يواجه فيروسًا أكثر صعوبة من فيروس نقص المناعة البشرية؛ كونه يختبئ بهدوء داخل الخلايا بدلاً من خوض معركة فورية ضارية مع جهاز المناعة، ثم يتطور بسرعة لا تصدق، وغالبًا ما يخلق متغيرات متعددة داخل المريض نفسه، فسيكون أحد أهم الأهداف. والعلماء يعتقدون فعلًا أن لديهم خارطة طريق للقاح.
ديريك كاين، الأستاذ بمعهد اللقاحات البشرية في جامعة ديوك، يقول إن الباحثين الآن أمامهم طريق واضح لإعادة إنتاج المعركة ربما في وقت قصير بشكل غير مسبوق.
يقول كاين: "لا يزال سؤال المليون دولار هو ما إذا كان هذا سينجح أم لا، لكن نهج mRNA يمكن أن يقدم إجابة في وقت أقرب بكثير مما كان يعتقده أي شخص قبل بضع سنوات فقط".

وبينما لا يزال العالم يركز على إطلاق لقاحات كورونا، فإن السباق نحو الجيل التالي من لقاحات mRNA - التي تستهدف مجموعة متنوعة من الأمراض الأخرى - آخذ في الازدياد بالفعل.
لدى موديرنا وبيونتك تسعة مرشحين في مرحلة التطوير أو التجارب السريرية المبكرة. هناك ما لا يقل عن ستة لقاحات mRNA ضد الإنفلونزا قيد التنفيذ، وعدد مماثل ضد فيروس نقص المناعة البشرية، بخلاف لقاحات نيباه وزيكا والهربس وحمى الضنك والتهاب الكبد والملاريا.
أوغو شاهين يذهب أبعد من ذلك. "نحن أمام تحول جذري دون أدنى شك. التأثير سيتجاوز ما نعرفه بالفعل. "هناك الكثير من الأشياء التي يمكننا القيام بها. هذا ليس مجرد بديل. سنبتكر ابتكارات طبية جديدة أخرى لن تكون ممكنة لولا ذلك".

تدور القصة نفسها عبر مئات المجالات العلمية المختلفة. 2020 فتح الأبواب على مصراعيها. لا يقتصر الأمر على أن لقاحات كورونا قد أثبتت صحة تقنية mRNA كنهج علمي؛ بل إلى بناء شبكة تنظيمية وتصنيعية واسعة لتقنية جديدة تمامًا في أقل من عام، قادرة على إنتاج مليارات الجرعات سنويًا.
بمعنى ما، أنشأت جائحة كورونا البنية التحتية لمستقبل mRNA التي يعد الباحثون بأنها ستكون أنظف وأسرع من الطرق التقليدية، في قيمة مضافة كان من الممكن أن تستغرق سنوات لتطويرها.
وبسبب هذا، فإن عدد المشاريع الجديدة ينفجر. تقرير حديث من Roots Analysis أحصى أكثر من 150 لقاحًا من mRNA وأنواع العلاج الأخرى قيد التطوير. إذا كان mRNA حقًا حقبة جديدة في علم اللقاحات، فمن المحتمل أن نعرف في المستقبل القريب جدًا، من العدد الهائل من الأدوية التي سيتم اختبارها.
Ziphius Vaccines، شركة بلجيكية صغيرة تأسست في 2019 للتركيز على علاجات mRNA للسرطان، تقول إنها تختبر عشرة أهداف، بما في ذلك حمى الضنك والتهاب الكبد والتهاب الدماغ الذي ينقله القراد، وتأمل في الحصول على نتائج ما قبل السريرية لأربعة أهداف على الأقل بنهاية 2022. هذا مع شركة محدودة بمختبرات صغيرة وبلا تملك بنية تحتية. قارنها بالشركات الكبرى لتتوقع النتائج.
حتى عملية التصنيع المبسطة بالفعل لهذه اللقاحات قد تكون على وشك الانكماش أكثر - مما يتيح جعلها ليس أسهل فحسب، بل يمكن إطلاقها في أي مكان تقريبًا.
أحد المهندسين يقول: "انتقلنا من حجم ملعب كرة القدم إلى حجم دائرة نصف الملعب. الآن لا مانع من أن تصبح البنية التحتية أصغر وأبسط. يضيف ساخرًا: "ربما لا تحتاج إلا إلى سطح المكتب مستقبلًا".

يصف الباحثون تقنية mRNA بما يشبه "الرقاقة الدقيقة" في علوم الكمبيوتر. إذ تعد بأداء نفس مهمة اللقاحات التقليدية، لكن بشكل أسرع، وبجزء بسيط من التكلفة. فيما تسميها موديرنا "برمجيات الحياة" أو "نظام التشغيل" للطب.
دانيال أندرسون، باحث العلاج بالـ mRNA في معهد ماساتشوستس للتكنولوجيا يصف حجم التغيير بقوله: "السرعة مذهلة. يمكن أن تطرأ الفكرة على رأسك في الصباح، ثم تصنع نموذجًا أوليًا للقاح بحلول المساء".
وبعد ما يقرب من 20 عامًا، اللقاحات التي أتاحها عمل كاريكو حولتها إلى شخصية علمية مشهورة، بالدرجة التي رشحها معها المؤسس المشارك لموديرنا ديريك روسي، وعالم الأحياء البريطاني ريتشارد دوكينز، للحصول على جائزة نوبل.
 موضوعات متعلقة
موضوعات متعلقة